Урок химии в 9-м классе. Тема: "Металлы. Железо. Строение атома, физические и химические свойства"
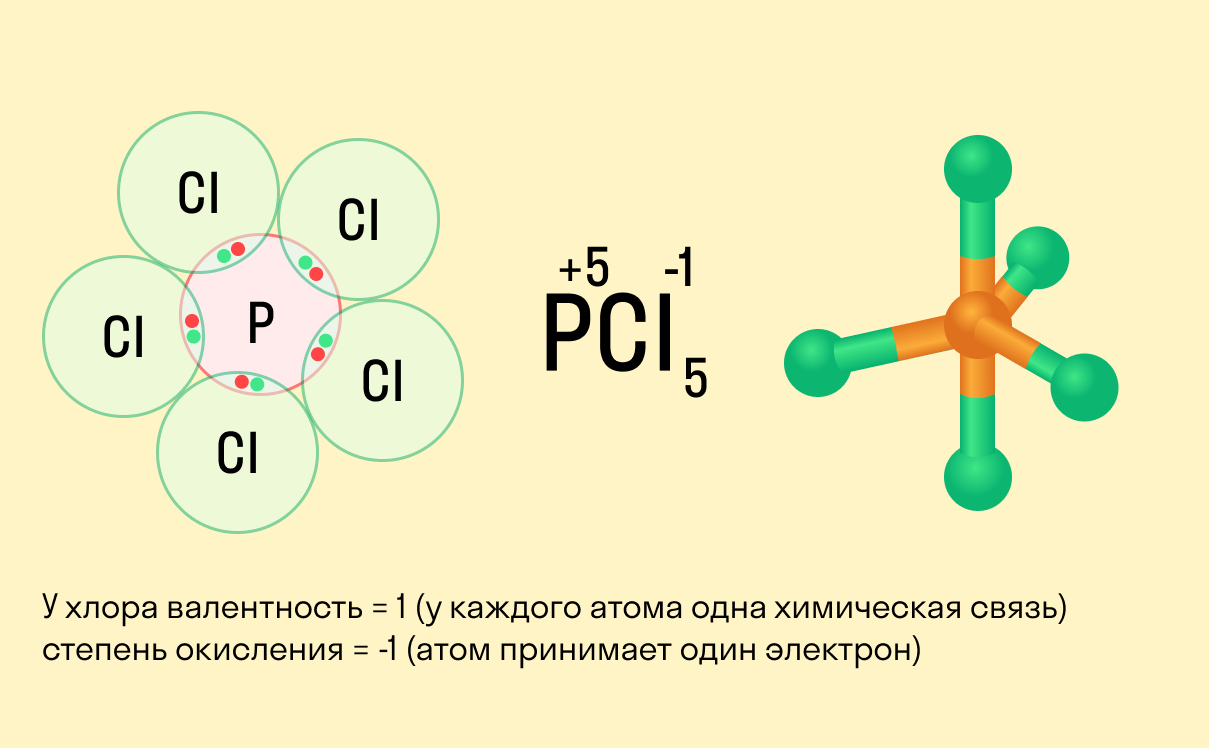
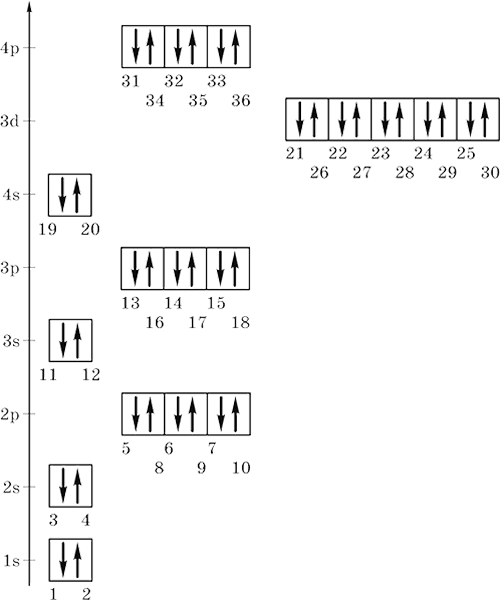
Железо имеет 26 электронов, заполним электронные оболочки в описанном выше порядке:. Атомы железа в соединениях имеют степени окисления 6, 5, 4, 3, 2, 1, 0, -1, Степень окисления - это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная электроны несут отрицательный заряд , если заряд уменьшается, то степень окисления положительная. Валентность железа характеризует способность атома Fe к образованию химических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами.

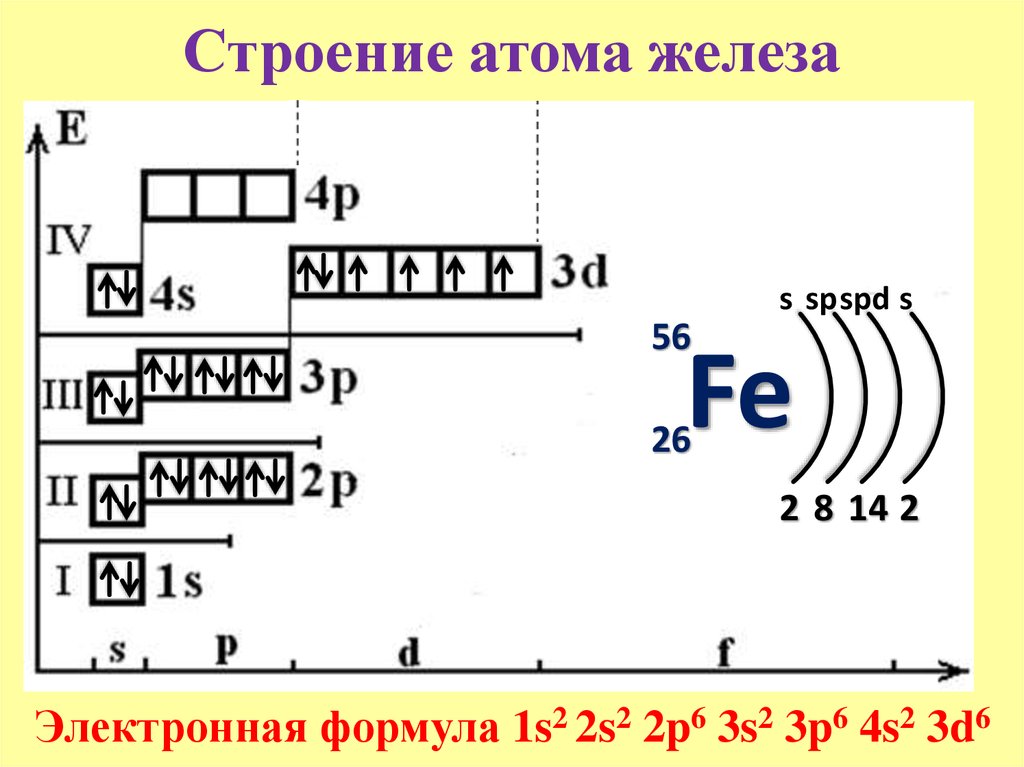

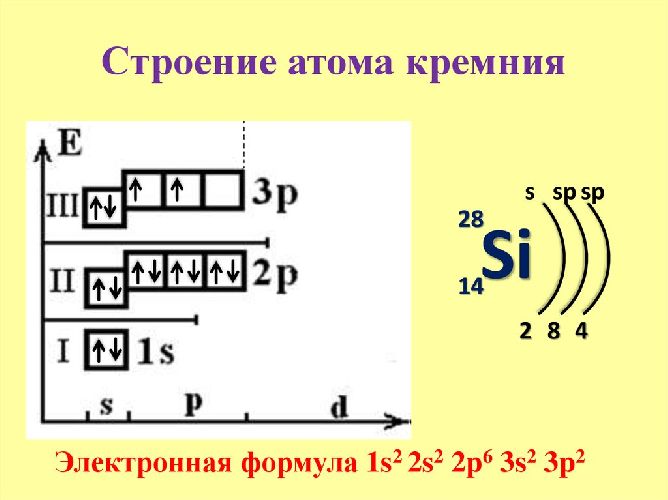

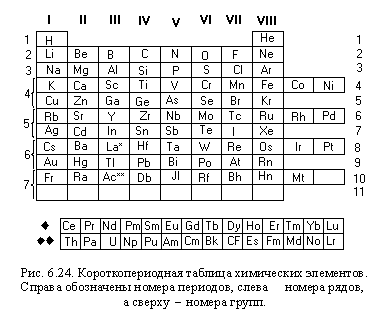




Железо в химии обозначается Fe от лат. По одной из версий, ferrum происходит от fars — быть твердым. Это элемент восьмой группы по прежней классификации — побочной подгруппы 8 группы четвертого периода периодической системы Д. Относится к классу металлов. Атомный номер Атомная масса 55,8.
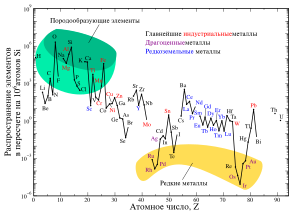
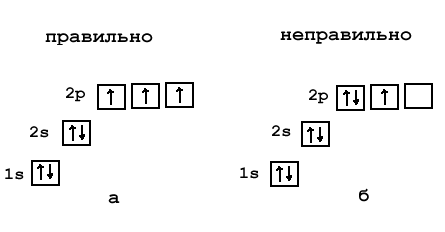
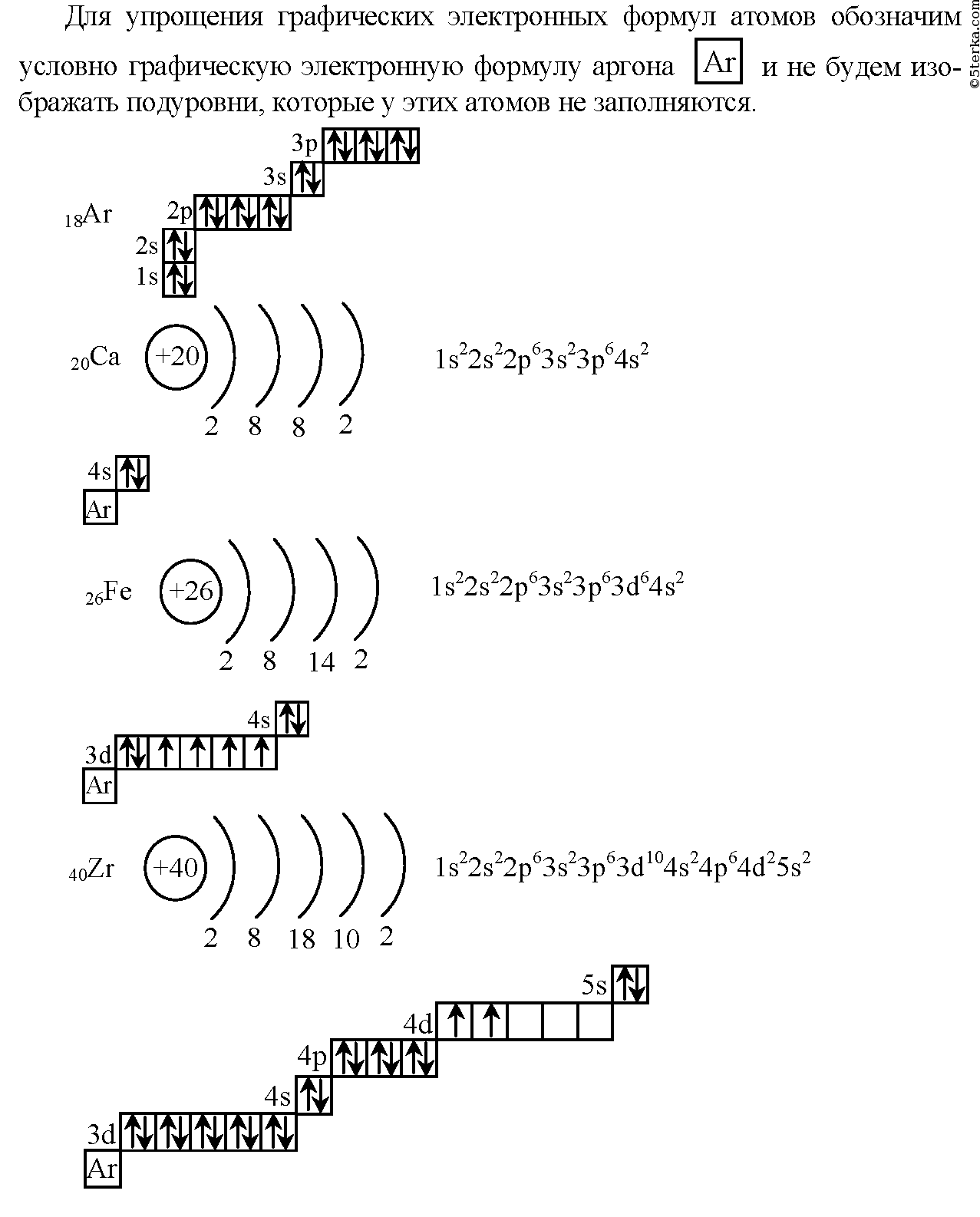

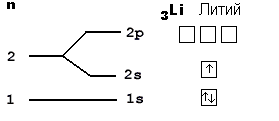
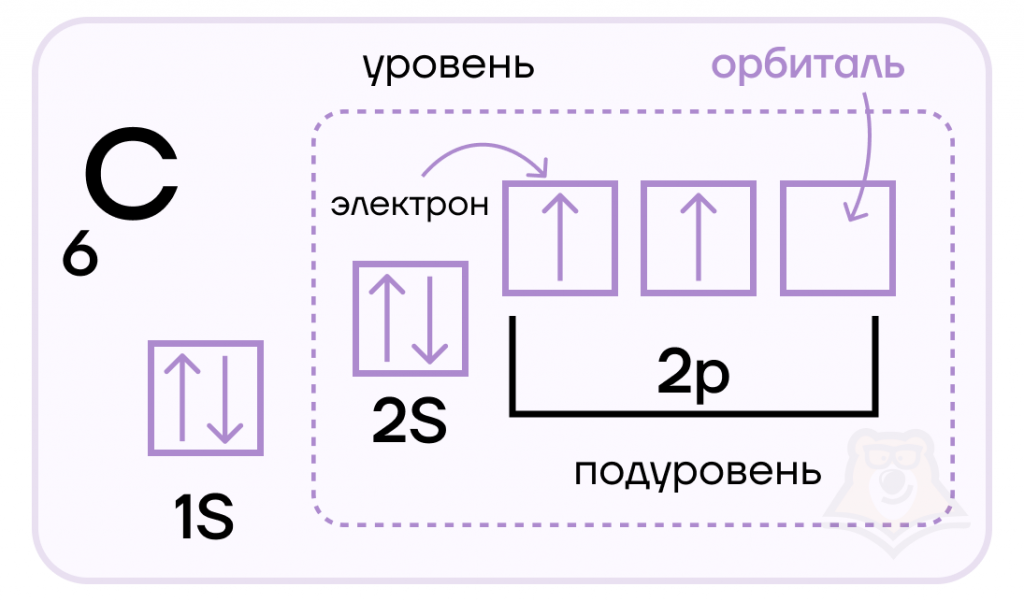


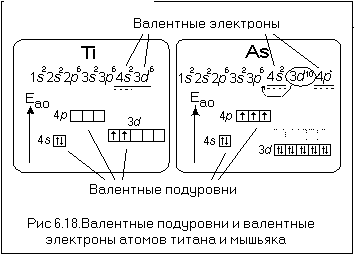
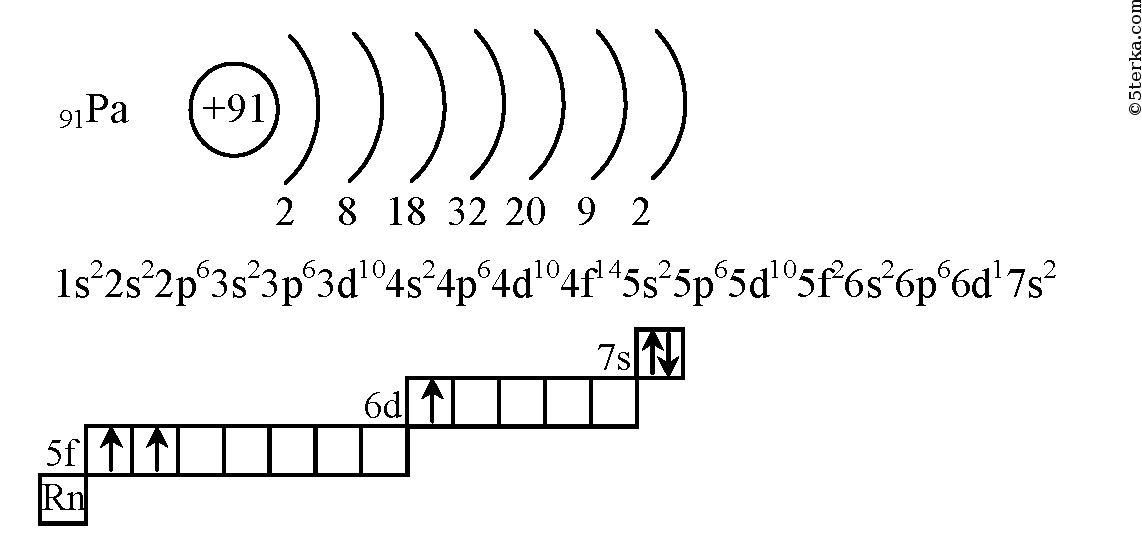
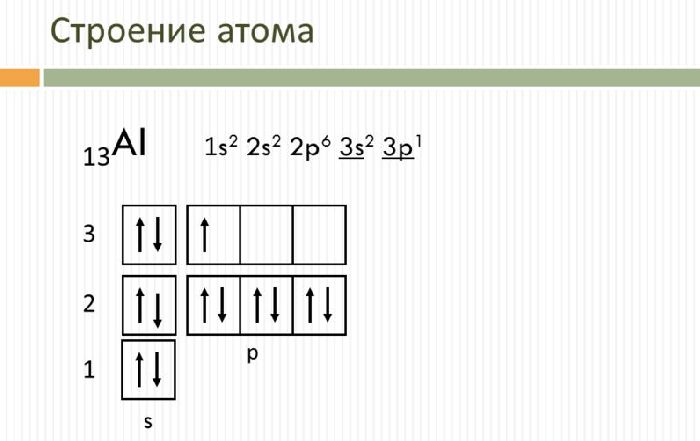
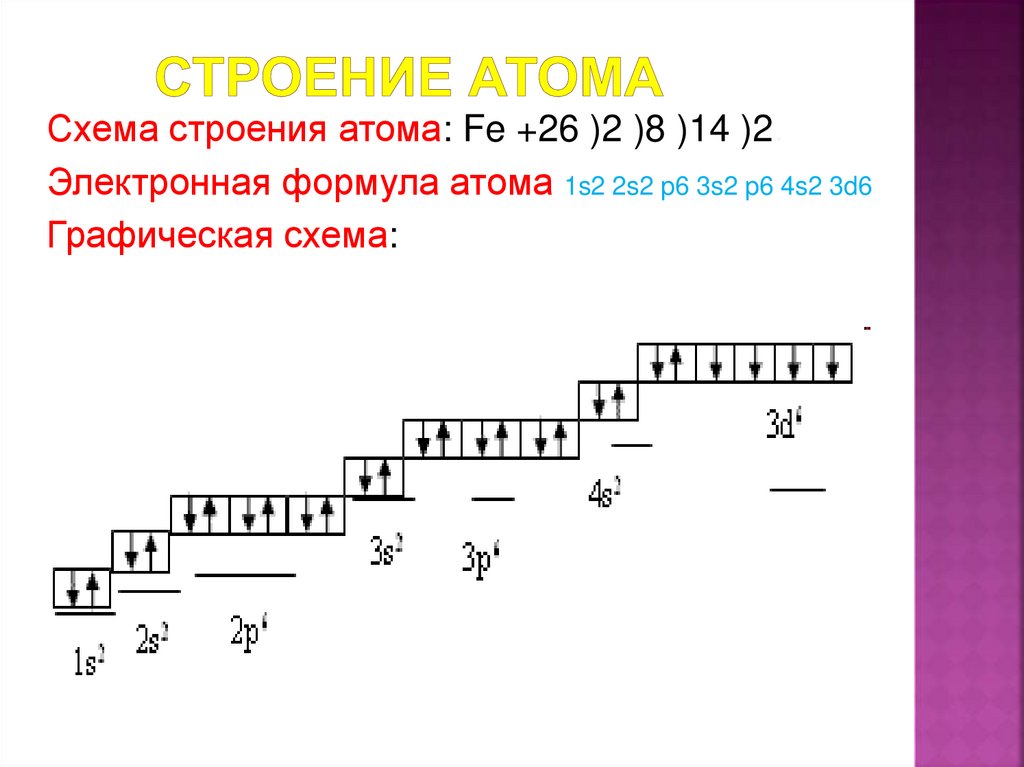
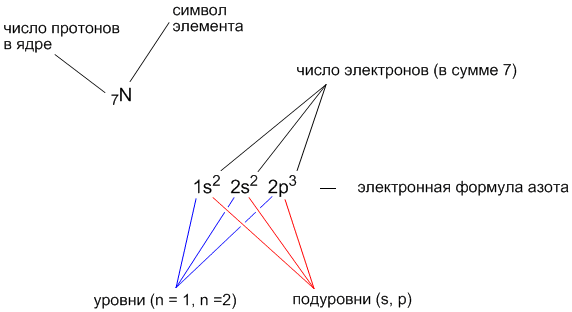
Электронная схема, формула электронной конфигурации и электронно-графическая схема его атома имеют вид:. Железо относится к d -элементам. В неокисленном состоянии железо изредка встречается в метеоритах в составе сплава с кобальтом и никелем.